耀海生物获悉,北京诺思兰德生物技术股份有限公司(以下简称:诺思兰德),继7月12日创新药NL003项目III期临床试验溃疡适应症获得NDA受理申请后,该项目再次迎来突破性进展。
8月16日,诺思兰德研发的“重组人肝细胞生长因子裸质粒注射液”(代号NL003)治疗下肢缺血性疾病III期临床试验静息痛适应症按既定计划揭盲,主要指标符合预期。初步结果表明:主要终点指标180天疼痛完全消失率结果,NL003组显著优于安慰剂对照组(p<0.0001);本品安全性良好,未发现与药物相关的严重不良反应。
NL003III期临床试验主要针对CLI,分为溃疡(Rutherford 5级)和静息痛(Rutherford 4级)两个适应症分别开展试验。试验采取随机、双盲、安慰剂、平行对照研究机制,以北京协和医院血管外科为组长单位,在全国共24家医院开展临床研究。其中溃疡适应症入组242例、静息痛试验入组302例。溃疡适应症已于2024年2月率先完成试验,并已于7月份正式获得CDE新药注册申请(NDA)受理,是我国首个申报NDA的裸质粒型基因治疗药物。
本次静息痛适应症揭盲后,还需根据方案及统计分析计划的规定开展全面深入分析,并完成临床试验总结报告。公司正同步开展该适应症的新药上市许可申请资料的撰写工作,并将积极与药监部门沟通申报事宜,计划本年内提交生物制品许可申请(BLA)。
对于重要战略合作伙伴诺思兰德取得的又一里程碑进展突破,耀海生物表示热烈祝贺的同时,也深受鼓舞振奋!
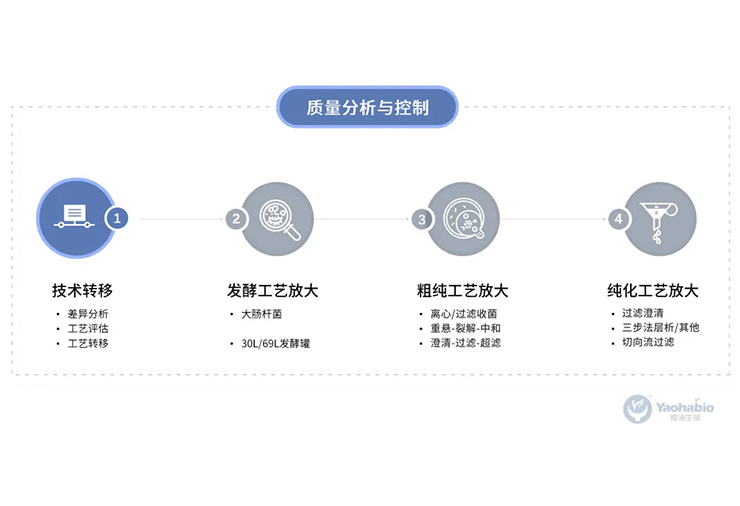
作为中国生物医药产业蓬勃发展的亲历者,耀海生物深耕微生物表达体系CRDMO服务多年,始终坚持创新发展,已搭建了行业领先的一站式CRDMO服务平台,业务涵盖“重组质粒、重组蛋白/多肽、纳米抗体、核酸药物及新型重组疫苗”等,坚定不移地提高和完善研发、生产、质量管理与控制服务体系。目前,已成功交付两百余个项目,贯穿早期研究、IND新药临床申报、临床样品GMP生产和商业化生产的全生命周期。
未来,公司将继续加强技术创新能力,完善和优化公司合规服务保障体系,以多维度的技术平台和全球化的服务标准,为全球客户提供更全面、更高端的研发制造服务。
关于诺思兰德
北京诺思兰德生物技术股份有限公司成立于2004年,是一家专业从事基因治疗药物、重组蛋白质类药物和眼科用药物研发、生产及销售的创新型生物制药企业。公司坚持以临床需求为导向,依托自主核心技术平台,主要致力于心血管疾病、代谢性疾病、罕见病和眼科疾病等领域生物工程新药的研发和产业化。
公司药品研发管线丰富且具有较高的成熟度,目前在研11个生物工程新药对应13个适应症,并已有3个进入临床研究阶段。除了NL003,其注射用重组人白细胞介素11(代号NL002)已进入III期临床,注射用重组人胸腺素β4(代号NL005)正在开展II期临床研究;多个眼科药品种陆续开发上市。公司拥有授权专利22项,先后承担国家级“重大新药创制”课题8项。