在重组蛋白等生物制品的小试工艺放大至生产规模时,耀海生物会评估以下变化可能导致的工艺放大风险:①培养基灭菌方式改变;②增加一级或多级种子罐,传代次数改变;③培养过程中传质、剪切作用不同;④补料方式存在差异(如泵的准确性);⑤适用于不同处理批量的离心和破碎设备不同;⑥大批量衍生的配液/储液特殊需求。以上变量可能对目标物质的产量、收率、稳定性造成影响。
因此,在小试工艺打通后,我们建议至少1批中试放大生产进行工艺的调整,目的是保证小试工艺至生产阶段的成功转移。
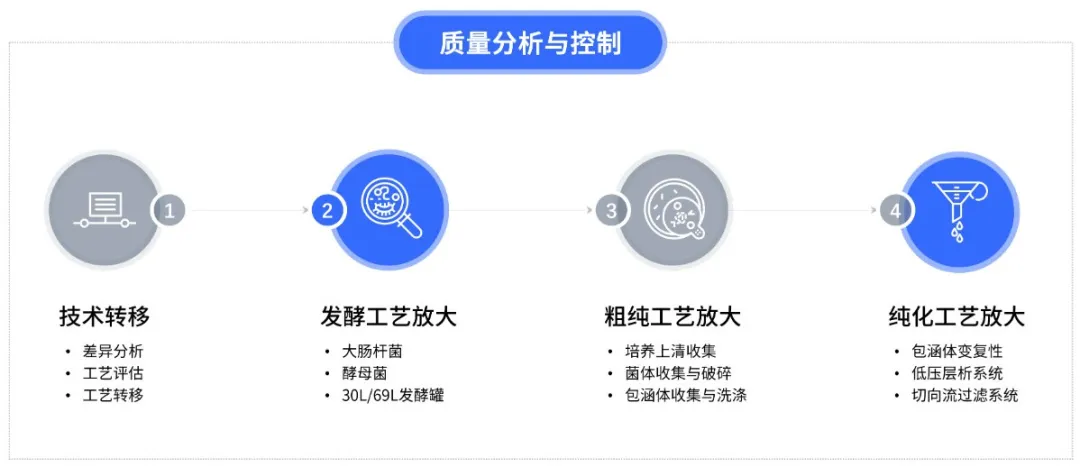
基于十余年微生物表达体系重组蛋白/质粒DNA生产及服务经验,耀海生物搭建了成熟完善的GMP-like级中试放大服务平台。截至目前,公司已成功服务了多个I-III期临床项目。耀海生物GMP-like级中试放大平台可用于小试工艺的优化,降低工艺放大的风险。制备的中试样品也可用于分析方法开发、稳定性预实验、制剂处方开发和制剂工艺开发试验等。
耀海生物GMP-like级中试放大平台拥有30L/69L发酵体系,并匹配不同规格的层析系统。耀海生物GMP-like级中试放大平台可满足30L/69L发酵规模下的工艺评估、工艺重现、工艺优化、中试样品生产等需求。我们能够高质量完成重组蛋白原液工艺的放大、优化和转移,向客户交付完整的中试放大报告,高效率推动CDMO项目的开发进程。
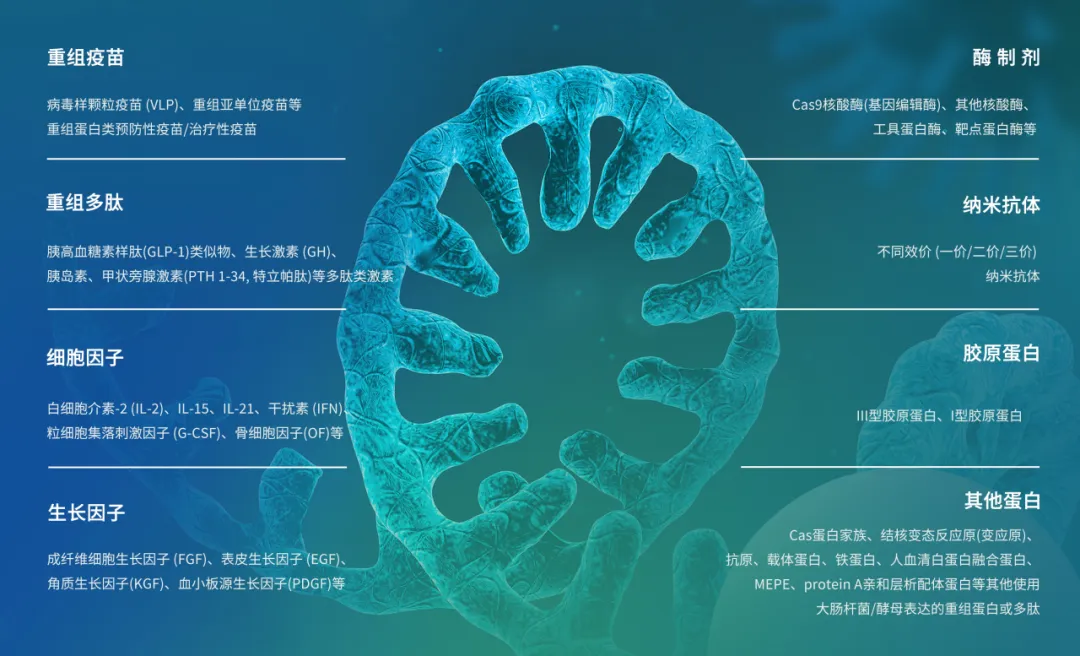
耀海生物中试放大平台可服务的重组蛋白制品
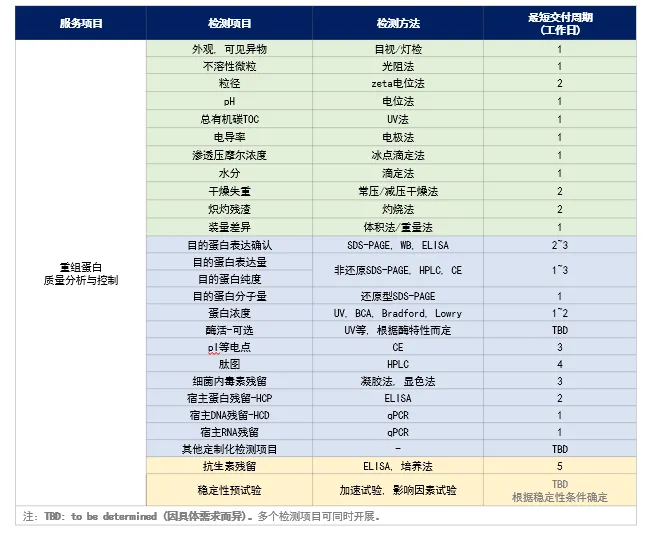
服务详情
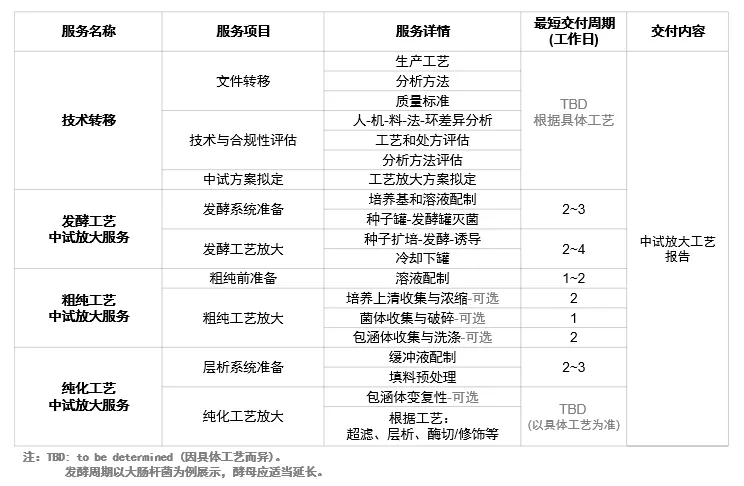
重组蛋白质量分析与控制
中试放大服务特色
1.完善的中试放大服务平台
耀海生物GMP-Like级中试原液车间,涵盖30L/69L发酵罐,匹配对应规模的离心、高压均质和低压层析设备,高效完成小试工艺放大。
2.多品种工艺放大经验
耀海生物团队全流程贯彻QbD理念,已成功实现多品类重组蛋白制品工艺放大与工艺转移,覆盖病毒样颗粒疫苗(VLP)、重组亚单位疫苗、纳米抗体、抗体片段、胰岛素、细胞因子、生长因子、酶制剂、胶原蛋白等。
3.质量合规保障平台支撑
专业的QC团队协助完成样品的检测,有效保证质量标准;
QA与注册团队协助评估工艺过程与质量标准的合规性,如宿主来源、无动物源、抗生素类型、毒性或致敏性、纯度、工艺过程残留等,全流程符合注册申报需求。
4.一站式CDMO服务平台支撑
基于超十年的多品种生产及服务经验,耀海团队贯彻全流程产业化理念,能够保证小试工艺、中试工艺稳定放大至生产水平。