ICH Q10指导原则将药品的生命周期分为4个阶段:药品研发、技术转移、商业化生产、产品终止。其中技术转移是药品生命周期的重要一环,是连接药品研发和商业化生产的承上启下的关键环节。
技术转移主要包括生产工艺、中间体控制、原辅料质量标准、检测方法及其他与产品质量相关联的技术与方法。技术转移的主要目标是实现研发与生产之间或不同生产场地之间产品及相关知识的转移,包括MAH与CDMO、CMO、CRO企业间的转移,以实现产品的持续稳定生产。
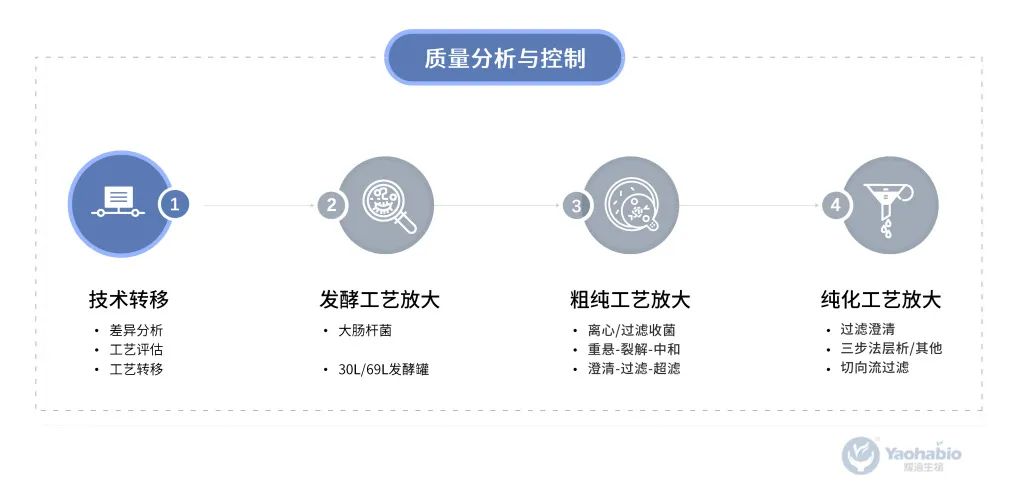
耀海生物依据《中国药典》2020版、ICH Q10、WHO、PDA TR65、ISPE等技术转移指南的理解与成熟服务经验,建立了从小试工艺开发、中试放大至GMP生产阶段(原液及制剂)的技术转移管理办法。
耀海生物始终明确技术转移流程,并基于质量源于设计(QbD)理念,对转移过程进行法规方面和质量管理的全面风险评估。耀海生物时刻加强药品全生命周期管理,确保技术转移的成功,充分保证不同客户对药品的安全、有效和质量可控等多种个性化需求。

服务详情
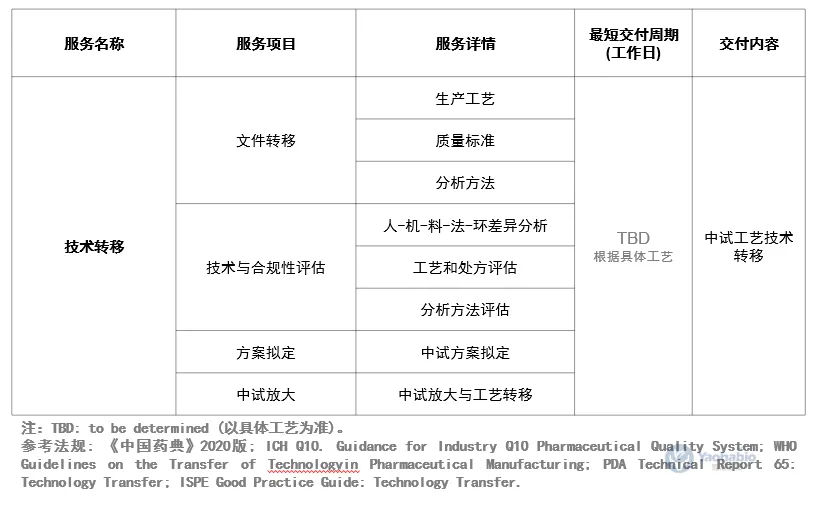
服务特色
1、丰富的工艺转移经验
我们会充分评估小试工艺流程、质量分析方法和质量标准的完整性和可行性,以期快速为客户提供全面的工艺转移解决方案。
2、合规性保障平台
常见合规性相关影响因素有宿主来源、无动物源、抗生素类型、毒性或致敏性、纯度、工艺残留等。
耀海生物会基于过往服务经验及法律法规要求,在工艺转移过程中进行合规性评估与管理,使客户项目全流程符合注册申报需求。
3、专业的项目管理团队
耀海生物拥有精于发酵、纯化工艺转移和放大的专业PM管理团队。我们能够快速识别和控制项目风险,全周期推动项目的运行。
技术转移关键参数
技术转移过程中有两个需要注意的难点。
其一,是因为客户与CDMO服务商设备型号不一致,进行工艺转移或规模放大的参数转换的过程中需要CDMO服务企业的大量参数转移经验,才能保证项目的顺利转移。例如发酵罐和离心机,不同品牌发酵罐径高比、搅拌叶分布和最大转速有所差异,可以通过控制通气、转速和溶氧量等关键参数,完成工艺的验证和放大。另外,不同的离心设备(台式、落地、筒式或碟式)适用于处理不同体积/批量的样品,因此在放大过程中,相当一部分的工艺要进行离心设备的转换,关键的离心工艺参数包括转速、进料和排渣时间(碟式)。耀海生物具有十余年多品种生产服务经验,目前对主流设备间参数转移已具备体系化服务经验。
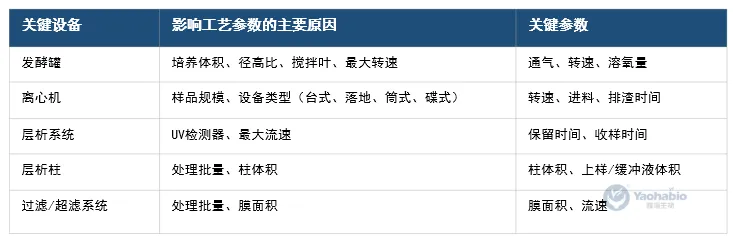
需要注意的另一个难点是CDMO服务商与客户设备型号基本一致的条件下,仅对客户工艺进行规模放大的参数转换。例如层析纯化时,将柱高和柱效保持在可控区间内,维持原有工艺的保留时间、载量和洗脱条件(线性流速),CDMO服务商需要根据实际放大倍数调整柱体积和上样体积。在过滤或超滤时,CDMO服务商则需要凭借服务经验、结合实际放大规模改变膜面积、控制流速。
基于100+质粒DNA/重组蛋白/多肽CMO服务经验,耀海团队积累了多种品牌、性能、型号的设备相关工艺转移经验,可快速识别并调整关键设备参数,高效完成小试工艺的调整和放大。
星耀小Tip:
工艺放大倍数建议在10倍以内,建议开展至少1批中试规模的放大,以调整生产工艺,控制工艺放大的风险。